Плавкие предохранители. Сила тока в каком-либо участке цепи определяется по закону Ома сопротивлением участка и напряжением между его концами. При заданном напряжении она тем меньше, чем больше сопротивление данного участка. Так, например, сопротивление обычных лампочек накаливания сравнительно велико (сотни ом), и поэтому сила тока в них получается малой (несколько десятых долей ампера).
Если соединить провода помимо лампочки, то получится участок с очень малым сопротивлением и ток может сделаться весьма большим. Говорят, что в этом случае имеет место короткое замыкание. Коротким замыканием называют вообще всякое замыкание источника тока на очень малое сопротивление. Развивающиеся при коротком замыкании большие токи чрезвычайно опасны из-за раскаливания проводов, а также крайне вредны для источника тока.
Для предохранения проводов от короткого замыкания служат плавкие предохранители. Это – тонкие медные проволочки, или, еще лучше, проволочки из легкоплавкого металла (например, свинца), вводимые последовательно в цепь тока и рассчитанные таким образом, чтобы они плавились при силе тока, превышающей то значение, на которое данная цепь рассчитана. На рис. 99 показано действие предохранителей. При замыкании проводов электрической лампочки куском толстой медной проволоки 1 (короткое замыкание) предохранитель 2 мгновенно плавится и цепь размыкается.
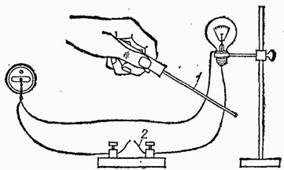
Рис. 99. При коротком замыкании медным стержнем 1 плавкий предохранитель 2 расплавляется и размыкает цепь
Устройство наиболее употребительного «пробочного» предохранителя показано на рис. 100. Его название происходит от фарфоровой «пробки» 1, внутри которой помещается легкоплавкая проволока 2. Пробка, подобно цоколю лампочки, ввинчивается в патрон предохранителя 3 и после каждого короткого замыкания заменяется новой. Обычно предохранители или группы предохранителей ставятся при вводе тока в дома и, кроме того, при вводе в каждую квартиру; нередко предохранителями снабжены и отдельные штепсели. Устройство штепсельного предохранителя показано на рис. 101. Предохранитель отдельного штепселя должен плавиться при токе 3-5 А, предохранитель в квартире – при токе 15-20 А, а предохранитель в доме – при значительно больших токах, в несколько сот ампер.
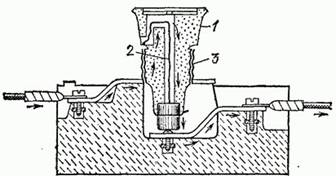
Рис. 100. «Пробочный» предохранитель: 1 – фарфоровая «пробка», 2 – легкоплавкая проволока, 3 – патрон предохранителя
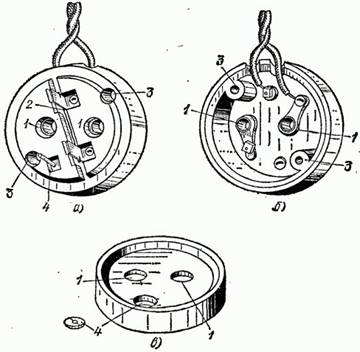
Рис. 101. Штепсельная розетка с предохранителем: а) вид сверху раскрытой штепсельной розетки; б) вид со стороны стены; в) крышка; 1 – гнезда для вилки, 2 – плавкий предохранитель, 3 – отверстия для шурупов, прикрепляющих штепсельную розетку к стене, 4 – приспособление для закрепления крышки











Комментарии: (0)